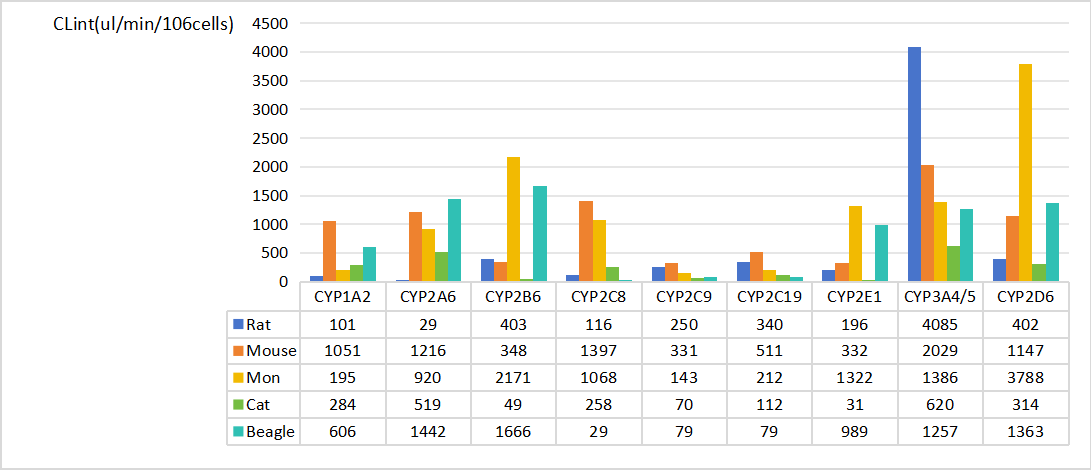
药物代谢评价技术服务
一、模型简介
药物代谢是指药物在生物体内经过一系列生物化学转化过程,最终被转化为代谢产物并排出体外的过程。它是药物在体内发挥作用、维持药效和消除毒性的关键环节。药物代谢通常发生在肝脏,但也可能在其他组织(如肠道、肾脏、肺等)中进行。通过药物代谢,药物分子被转化为更易排泄的形式,同时其药理活性或毒性也可能发生改变。药物代谢的主要场所如下图:
肝脏:是药物代谢的主要器官,富含代谢酶(如CYP450、UGT等)。
肠道:肠道微生物和肠壁细胞也参与部分药物的代谢。
肾脏和肺:在特定情况下,这些器官也可能参与药物代谢。
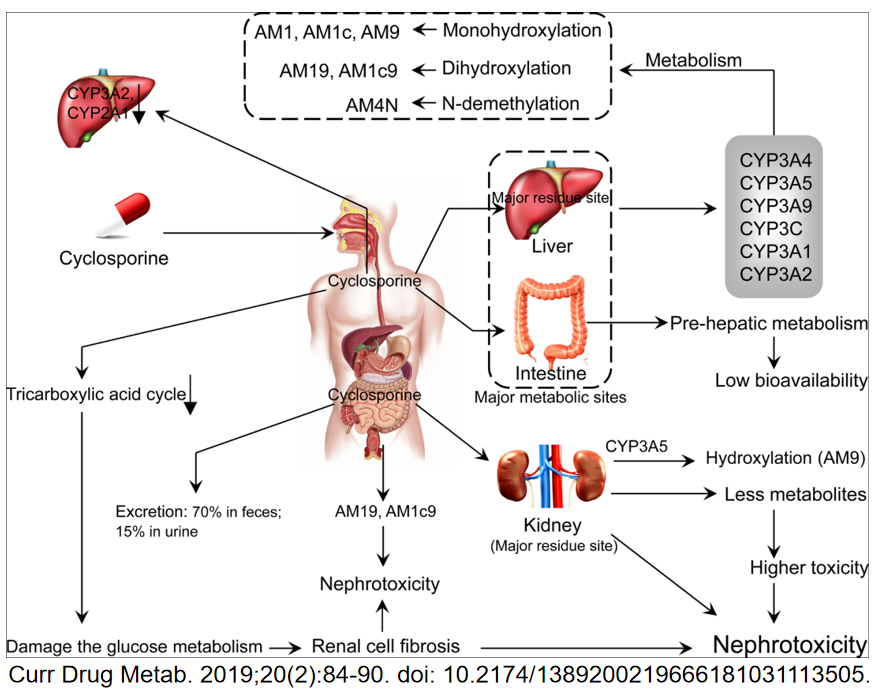
1、小分子化合物的代谢途径
小分子化合物是药物研发中最常见的类型,其代谢途径主要包括Ⅰ相代谢和Ⅱ相代谢:
Ⅰ相代谢:通过氧化、还原、水解等反应,将药物转化为更具极性的代谢产物。例如,对乙酰氨基酚通过CYP450酶系氧化为N-乙酰对苯醌亚胺(NAPQI)。
Ⅱ相代谢:通过结合反应(如葡萄糖醛酸化、硫酸化、谷胱甘肽结合)进一步增加代谢产物的极性,促进其排泄。例如,吗啡通过葡萄糖醛酸化生成吗啡-3-葡萄糖醛酸。
代谢产物鉴定:使用LC-MS/MS、NMR等高灵敏度技术鉴定代谢产物,并评估其药理活性或毒性。
代谢酶鉴定:确定参与代谢的关键酶(如CYP450、UGT等),并评估其基因多态性对药物代谢的影响
2、小核酸药物代谢途径
小核酸药物(如siRNA、反义寡核苷酸)的代谢途径与传统小分子化合物不同,主要包括以下方面:
代谢途径:小核酸药物主要通过核酸酶(如RNase H、核酸外切酶)降解为短片段,最终代谢为单核苷酸。例如,siRNA在体内被核酸酶降解为短片段,最终代谢为单核苷酸。
代谢产物鉴定:使用LC-MS/MS、凝胶电泳等技术鉴定代谢产物,并评估其药理活性或毒性。
代谢动力学研究:使用血浆、肝细胞等体外模型研究代谢动力学,并通过动物实验研究体内代谢动力学。
代谢酶鉴定:确定参与代谢的关键酶(如核酸酶、磷酸酶),并评估其活性对药物代谢的影响。
二、检测模型
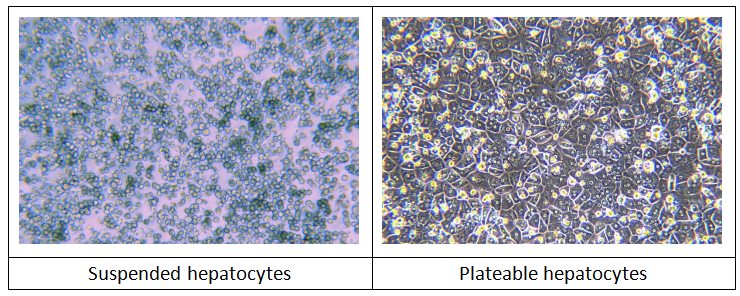
1、原代肝细胞
采用人、猴、犬、大鼠、小鼠等物种的原代肝细胞,模拟体内药物代谢环境,评估药物的代谢稳定性及代谢产物。
2、S9/肝微粒体
肝微粒体是肝细胞内质网的膜成分,富含Ⅰ相代谢酶(如细胞色素P450酶系,CYP450)和少量Ⅱ相代谢酶(如UGTs、ST等)。
主要应用:
Ⅰ相代谢研究:肝微粒体主要用于研究氧化、还原和水解反应,是Ⅰ相代谢的主要场所。例如,CYP450酶系能够将药物转化为更易排泄的形式。
代谢产物鉴定:通过LC-MS/MS等技术,可以鉴定药物代谢产物并评估其药理活性或毒性。
代谢酶鉴定:确定参与代谢的关键酶(如CYP450、UGT等),并评估其基因多态性对药物代谢的影响。
代谢动力学研究:通过体外孵育实验,研究药物的代谢半衰期(t1/2)和内在清除率(Clint)。
肝S9是肝组织匀浆后去除沉淀物的混悬溶液,包含完整的Ⅰ相和Ⅱ相代谢酶(如CYP450、UGTs、SULT等)。
主要应用:
复杂代谢产物研究:肝S9适合研究经过Ⅰ相和Ⅱ相代谢的复杂代谢产物,尤其适用于非CYP酶代谢途径的药物。
代谢产物鉴定:通过LC-MS/MS等技术,鉴定代谢产物并评估其药理活性或毒性。
代谢酶鉴定:确定参与代谢的关键酶(如核酸酶、磷酸酶等),并评估其活性对药物代谢的影响。
优势:酶种类齐全,适合代谢产物的系统定性研究,但酶活性较低,代谢产物生成量较少。
应用区别
酶种类:肝S9包含完整的Ⅰ相和Ⅱ相代谢酶,而肝微粒体主要富含Ⅰ相酶。
酶活性:肝微粒体酶活性较高,适合定量研究;肝S9酶活性较低,但酶种类更全。
应用场景:
当药物主要通过CYP酶代谢时,选择肝微粒体。
当药物涉及非CYP酶代谢或需要研究复杂代谢产物时,选择肝S9。
3、溶酶体
1) 药物研发与靶向治疗
溶酶体在药物研发中具有重要作用,尤其是在靶向治疗和克服耐药性方面:
靶向溶酶体药物:溶酶体因其独特的酸性环境和丰富的酶系统,成为药物靶向的重要对象。例如,天然产物重楼皂苷 D(Polyphyllin D, PD)通过靶向酸性鞘磷脂酶(SMPD1)诱导溶酶体膜通透性(LMP),触发肝癌细胞的溶酶体依赖性细胞死亡,并增强索拉非尼的抗肿瘤效果。
克服耐药性:肿瘤细胞中的溶酶体常通过富集药物(如索拉非尼)导致耐药性。通过开发溶酶体靶向药物,可以破坏溶酶体功能,释放药物并增强其疗效。
2)蛋白质降解技术
溶酶体在蛋白质降解技术中扮演重要角色,尤其是在基于溶酶体的蛋白质降解剂开发中:
CMA Chimera技术:通过分子伴侣介导的自噬(CMA)途径,将目标蛋白与溶酶体结合并降解。
3)代谢研究与疾病模型
代谢研究:通过分离溶酶体,研究其酶活性和代谢功能,揭示细胞内物质降解和回收利用的机制。例如,使用密度梯度超速离心法或免疫沉淀法分离溶酶体,结合质谱分析鉴定其蛋白质组成和功能。
疾病模型:溶酶体功能障碍与多种疾病相关,如神经退行性疾病、溶酶体贮积症和癌症。通过研究溶酶体在疾病中的作用,可以为疾病治疗提供新靶点。例如,在肝细胞癌(HCC)中,溶酶体通过调控自噬和化疗耐药性,成为治疗的重要靶点。
4)药物代谢与稳定性研究
溶酶体在药物代谢和稳定性研究中也具有重要应用:
药物代谢:溶酶体通过其水解酶系统参与药物的代谢和降解。例如,在眼科药物研发中,溶酶体通过降解药物影响其疗效和稳定性,研究溶酶体代谢途径有助于优化药物设计。
药物稳定性:通过体外模型(如肝微粒体、肝S9)研究药物在溶酶体中的代谢稳定性,评估其药代动力学特征和潜在毒性。
5) 细胞自噬与死亡调控
溶酶体在细胞自噬和死亡调控中发挥核心作用:
自噬调控:溶酶体通过自噬途径降解细胞内受损或多余的细胞器,维持细胞稳态。例如,在肿瘤治疗中,通过诱导溶酶体依赖性自噬,可以抑制肿瘤细胞生长。
细胞死亡:溶酶体膜通透性(LMP)的诱导可触发细胞死亡,为癌症治疗提供新策略。例如,通过靶向溶酶体膜,诱导肿瘤细胞死亡并增强化疗效果。
三、检测条件

液质联用仪
四、服务资质、条件与团队
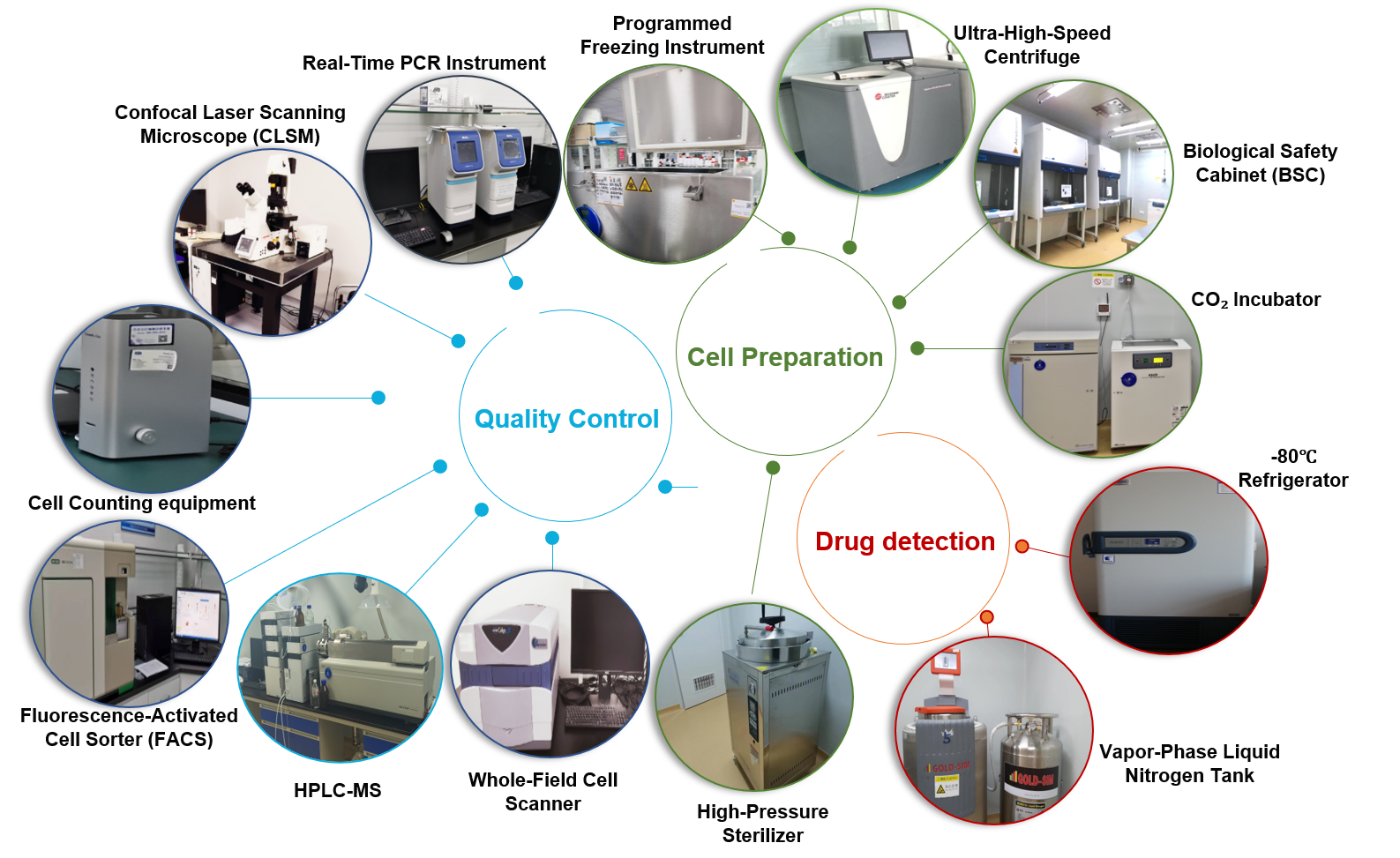
本公司按照GMP标准建设生物安全二级实验室,并完成卫健委备案,病原体范围:乙肝病毒、慢病毒等工具病毒、人体或动物样本。生物安全二级实验室配套检测设备、设施价值2000余万元,包括激光共聚焦、分选流式细胞仪、超高速离心机、实时荧光定量PCR仪等。技术团队包括美国医学与生物工程院院士、青年千人计划、深圳市高层次人才等;其中,周明博士,博士毕业于中科院武汉病毒研究所,从事肝脏研究究14年,获得国家自然科学基金、博士后基金、广东省科技厅、深圳市科创委等项目资助7项,发表第一作者或通讯作者SCI论文10余篇。

五、服务流程

六、服务案例
案例1 上海某生物医药公司
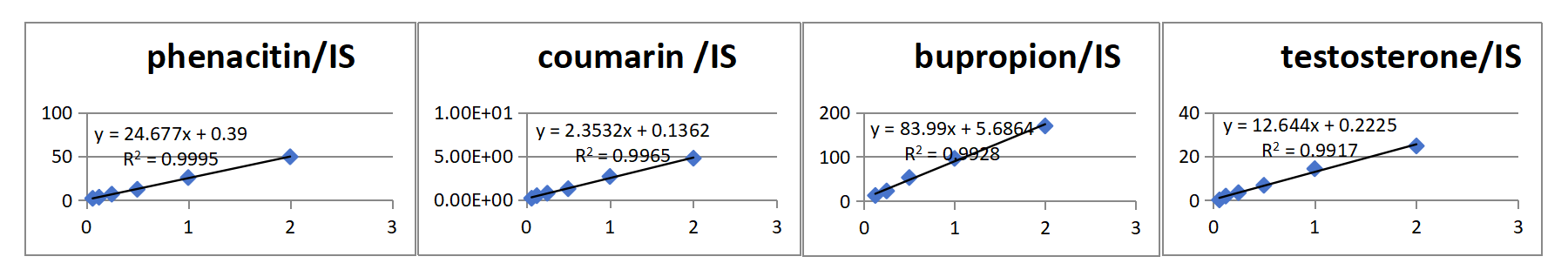
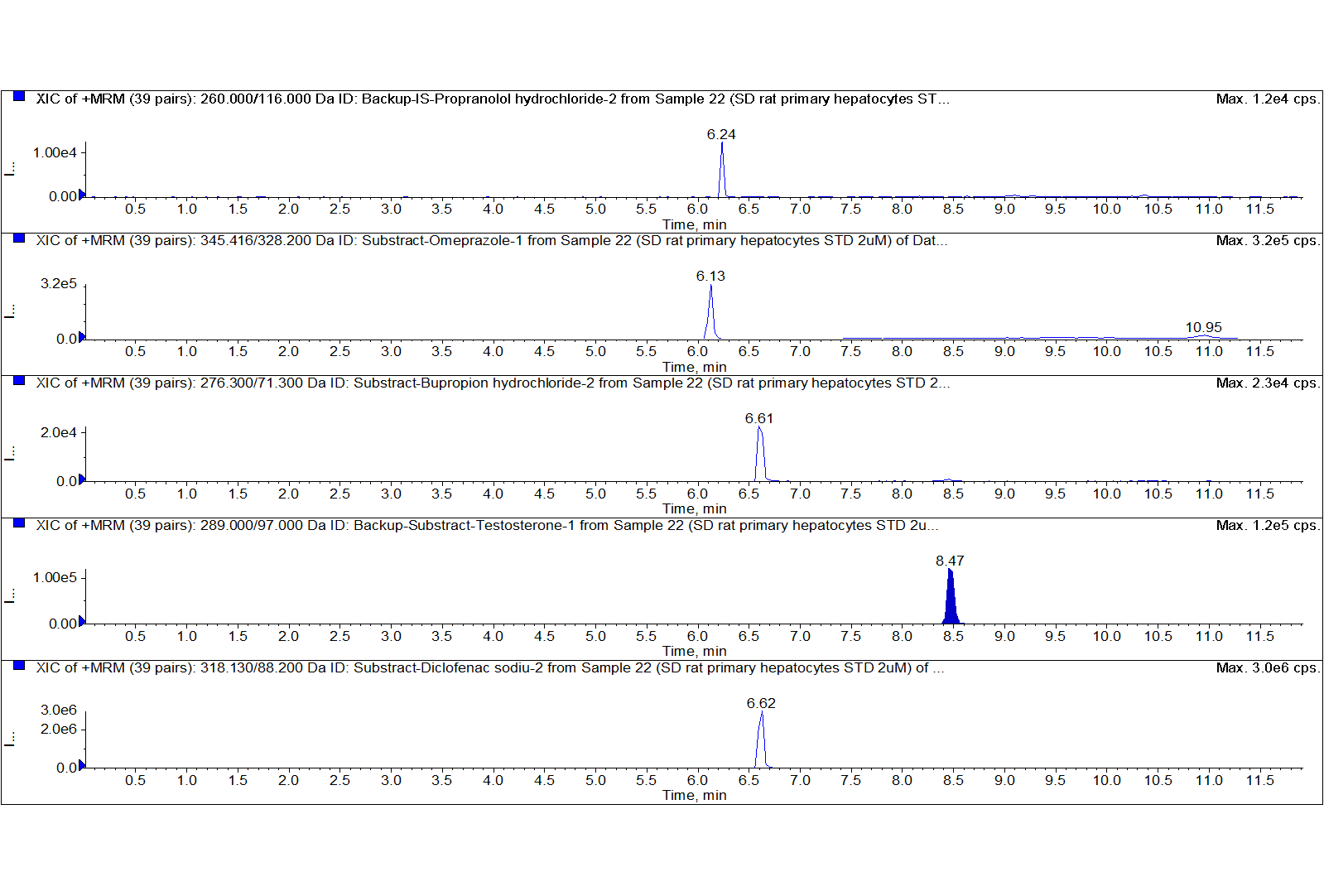
案例2 杭州某科研机构